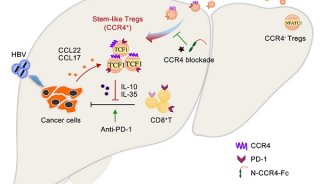
CCR4介導HBV相關肝癌浸潤Treg細胞研究取得進展
HBV感染是我國原發性肝癌最主要的致病因素。作為這種慢性感染性肝炎導致的腫瘤,HBV相關肝癌具有與其他類型截然不同的發病機制和治療特點,例如肝癌晚期一線藥物索拉非尼在HBV單陽性肝癌中療效不顯著。此外,HBV感染還與肝癌門靜脈癌栓等血管轉移密切相關。打破HBV相關肝癌的免疫耐受,尋求靶向T細胞免疫治療新靶點有重要的科研意義及臨床應用價值。
近期,中國科學院生物物理研究所楊鵬遠課題組、解放軍總醫院第五醫學中心等合作,在Journal of Hepatology發表研究論文Intratumoral stem-like CCR4+ regulatory T cells orchestrate the immunosuppressive microenvironment in HCC associated with hepatitis B,闡述瘤內CCR4介導調節性T細胞(Treg)促進HBV相關肝癌免疫逃逸新機制,揭示CCR4+ Treg亞群的干細胞樣表觀遺傳調控特征,為HBV相關肝癌的防治提供了新的理論基礎和干預策略。
生物物理所多年來持續關注HBV相關肝癌中負向免疫調節功能Treg細胞的聚集機制。前期研究發現,HBV通過活化TGF-β信號促進趨化因子CCL22表達,誘發Treg細胞遷移至腫瘤組織區域,介導免疫逃逸。在索拉非尼治療的HBV相關肝癌中激活TNFα/RIP1/NF-κB信號通路顯著上調CCL22,招募Treg細胞促進索拉非尼耐藥;拮抗CCL22信號通路可打破索拉非尼耐藥,有助于解決HBV相關肝癌治療中一線藥物耐藥的難題。HBV感染通過HBx促進ERK信號下游趨化因子CXCL8(IL-8)表達,通過其受體CXCR1在肝血竇內皮中特異激活肝內TGF-β信號,促進肝內Treg浸潤和血管轉移。
近期研究在HBV相關肝癌臨床標本及小鼠原位肝癌荷瘤模型等檢測到癌組織特異性浸潤的Treg細胞高表達趨化因子CCL22受體CCR4,并與HBV滴度及預后顯著相關。利用可接近染色質測序(ATAC-seq)及多數據庫平臺分析發現,這群腫瘤浸潤的CCR4+ Treg細胞在TCF7和PD-1染色質區域更加開放,顯著上調TCF7轉錄因子活性,表現出干細胞樣表觀遺傳調控特征。功能研究發現,相較CCR4- Treg,CCR4+ Treg免疫抑制功能更強,通過分泌高水平IL-10、IL-35等抑制殺傷性T細胞功能,促進腫瘤免疫逃逸。利用拮抗劑及自主研發合成的N端融合蛋白靶向CCR4治療可以顯著抑制腫瘤生長,與索拉非尼、PD-1抑制劑等聯用可打破藥物耐藥性,增強免疫治療效果。值得關注的是,這種靶向CCR4+ Treg能顯著抑制瘤內的免疫耐受,但不影響機體正常免疫組織中Treg細胞穩態的維持,避免免疫過度活化等副作用的發生。因此,CCR4可作為一種特異靶向HBV相關肝癌免疫逃逸和肝癌血管轉移的藥物治療靶點。
研究得到國家自然科學基金委、中科院和重慶國際免疫研究院的支持。
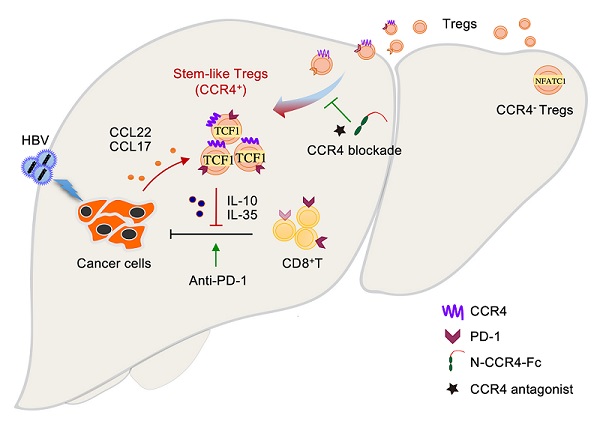
CCR4介導Treg促進HBV相關肝癌免疫逃逸新機制模式圖
-
科技前沿